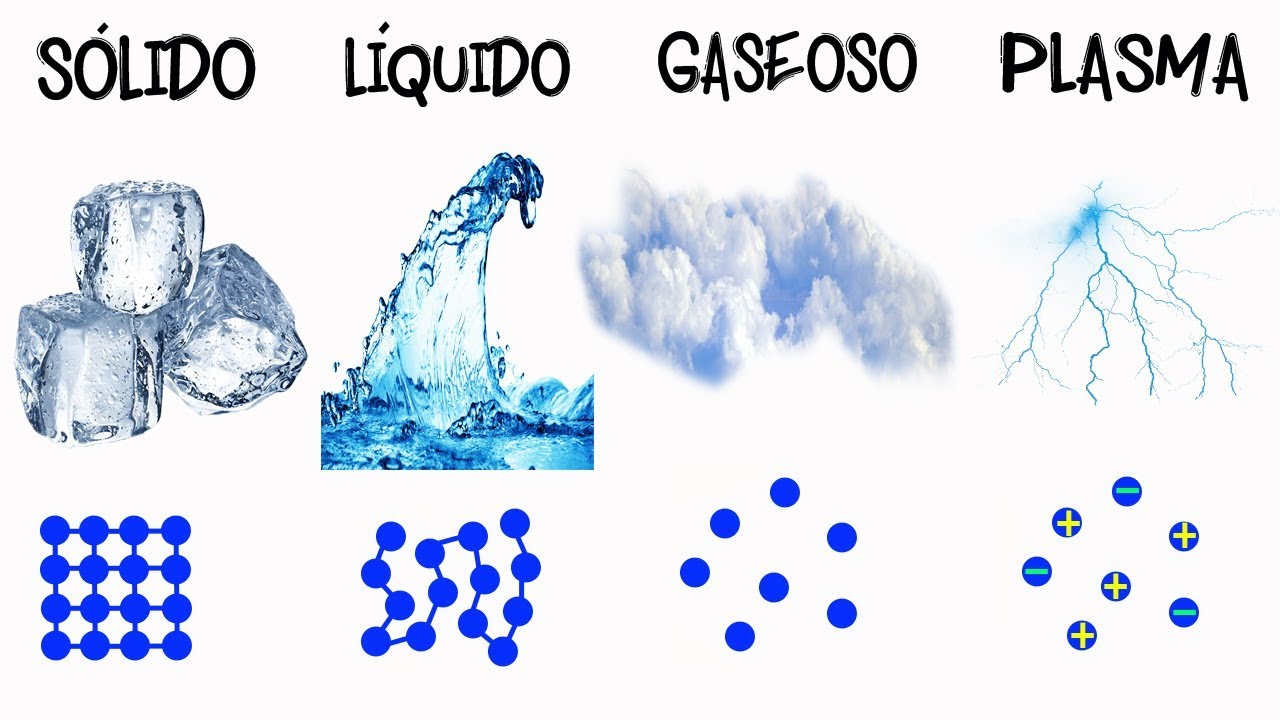
Estados de Agregación de la Materia: Características y Tipos Explicados
Introducción a los Estados de Agregación
¿Alguna vez te has preguntado por qué el agua puede ser líquida en un vaso, pero se convierte en hielo en el congelador? O ¿por qué al calentarla se transforma en vapor? Estos cambios son el resultado de lo que conocemos como estados de agregación de la materia. La materia, que es todo lo que nos rodea, puede existir en diferentes formas: sólida, líquida, gaseosa y, en algunos casos, incluso en estado plasmático. Cada uno de estos estados tiene características únicas que los diferencian entre sí. En este artículo, nos sumergiremos en cada uno de estos estados, exploraremos sus propiedades y descubriremos cómo y por qué ocurren los cambios entre ellos. ¡Prepárate para un viaje fascinante por el mundo de la materia!
Estado Sólido: La Estructura Firme
Comencemos con el estado sólido, que es quizás el más fácil de visualizar. Imagina un bloque de hielo: su forma es fija y no cambia a menos que lo derritas. En los sólidos, las partículas están muy juntas y vibran en su lugar, lo que les da una estructura definida. Esta rigidez es lo que permite que los sólidos mantengan su forma, incluso si los empujas o los aprietas. Además, los sólidos suelen ser más densos que los líquidos y gases, lo que significa que ocupan menos espacio en comparación con su masa.
Características de los Sólidos
Los sólidos tienen varias características notables. Por un lado, poseen un volumen y una forma definidos. Esto se debe a que las partículas en un sólido están organizadas en un patrón regular. Además, los sólidos son incomprensibles, lo que significa que no se pueden comprimir fácilmente. Si alguna vez has intentado aplastar un ladrillo, sabes exactamente a qué me refiero. Pero, claro, no todos los sólidos son iguales. Existen sólidos cristalinos, como los minerales, que tienen estructuras ordenadas, y sólidos amorfos, como el vidrio, que no tienen una estructura interna definida.
Estado Líquido: La Fluidez de la Materia
Ahora, pasemos al estado líquido. ¿Recuerdas cómo el agua puede adaptarse a la forma del recipiente que la contiene? Esto es lo que hace que los líquidos sean tan especiales. Las partículas en un líquido están más separadas que en un sólido, lo que les permite moverse libremente, pero aún están lo suficientemente unidas como para mantener un volumen constante. Imagina un río: el agua fluye y cambia de forma, pero siempre ocupa el mismo espacio. Esta capacidad de fluir es una de las características más distintivas de los líquidos.
Características de los Líquidos
Los líquidos tienen un volumen definido, pero no una forma fija. Esto significa que pueden adoptar la forma del recipiente en el que se encuentran. Además, son menos densos que los sólidos, lo que explica por qué los cubitos de hielo flotan en el agua. También son incomprensibles, aunque no tanto como los sólidos. Si alguna vez has intentado apretar un globo lleno de agua, sabes que puedes hacerlo, pero no mucho. Los líquidos también son excelentes conductores de calor, lo que significa que pueden transferir energía térmica de manera eficiente.
Estado Gaseoso: La Libertad en Movimiento
Ahora, hablemos del estado gaseoso. Si alguna vez has inflado un globo, has experimentado el gas en acción. En este estado, las partículas están tan separadas que se mueven libremente y se dispersan en el espacio. Esto significa que los gases no tienen ni forma ni volumen definidos; simplemente ocupan todo el espacio disponible. Imagina el aire en una habitación: no puedes verlo, pero está ahí, llenando cada rincón. Los gases son menos densos que los líquidos y los sólidos, y pueden comprimirse fácilmente.
Características de los Gases
Los gases tienen varias características que los hacen únicos. Como mencionamos, no tienen forma ni volumen definidos, lo que significa que pueden expandirse y contraerse según el espacio disponible. Esto es lo que permite que un aerosol se expanda al salir de la lata. Además, los gases son muy compresibles; si alguna vez has intentado comprimir el aire en una botella, sabes que puedes hacerlo sin mucho esfuerzo. A diferencia de los sólidos y líquidos, los gases son malos conductores de calor, lo que significa que no transfieren energía térmica de manera eficiente.
Estado Plasmático: El Cuarto Estado de la Materia
Finalmente, llegamos al estado plasmático, que es un poco más complicado de entender. El plasma es un gas ionizado, lo que significa que las partículas han perdido algunos de sus electrones y se comportan de manera muy diferente a los gases normales. Este estado se encuentra comúnmente en las estrellas, incluido nuestro sol. Imagina una bola de fuego: eso es plasma en acción. Este estado se produce a temperaturas extremadamente altas, donde la energía es suficiente para romper los enlaces entre electrones y núcleos atómicos.
Características del Plasma
El plasma es único porque es altamente conductor de electricidad y responde fuertemente a campos magnéticos. Esto lo convierte en un componente clave en la tecnología moderna, desde pantallas de plasma hasta fusiones nucleares. Además, el plasma emite luz, lo que lo hace visible en formas como relámpagos o auroras boreales. A diferencia de los otros estados de la materia, el plasma no tiene una forma o volumen definidos y puede expandirse o contraerse como un gas, pero con propiedades eléctricas adicionales.
Cambios de Estado: De Uno a Otro
Ahora que hemos cubierto los estados de agregación, es importante entender cómo se producen los cambios entre ellos. ¿Te has preguntado alguna vez cómo el agua se convierte en vapor o en hielo? Estos cambios de estado son el resultado de la transferencia de energía. Por ejemplo, cuando calientas agua, las partículas adquieren más energía y comienzan a moverse más rápido, lo que puede llevar a la vaporización. Por otro lado, al enfriar el agua, las partículas pierden energía, se acercan y eventualmente se convierten en hielo. Este proceso se conoce como congelación.
Ejemplos de Cambios de Estado
Hay varios cambios de estado que son importantes de conocer. La fusión es el proceso por el cual un sólido se convierte en líquido, como cuando el hielo se derrite. La solidificación es el proceso inverso, donde un líquido se convierte en sólido, como cuando el agua se congela. La evaporación es cuando un líquido se convierte en gas, mientras que la condensación es el proceso inverso, donde un gas se convierte en líquido. Y por último, la sublimación es cuando un sólido se convierte directamente en gas, como el hielo seco que se convierte en vapor sin pasar por el estado líquido.
Conclusiones y Reflexiones Finales
Los estados de agregación de la materia son fascinantes y nos muestran cómo la energía y la temperatura pueden influir en el comportamiento de las partículas. Desde los sólidos rígidos hasta los gases en expansión y los plasmas vibrantes, cada estado tiene sus propias características y propiedades. Comprender estos conceptos no solo es crucial en la ciencia, sino que también nos ayuda a apreciar el mundo que nos rodea. ¿Alguna vez has pensado en cómo estos cambios de estado afectan tu vida diaria? Desde el agua que bebes hasta el aire que respiras, la materia está en constante transformación.
Preguntas Frecuentes
- ¿Por qué los sólidos tienen una forma definida? Los sólidos tienen una forma definida porque sus partículas están organizadas en un patrón regular y vibran en su lugar.
- ¿Qué sucede con las partículas durante la evaporación? Durante la evaporación, las partículas en un líquido adquieren suficiente energía para superar las fuerzas que las mantienen unidas y se convierten en gas.
- ¿Es posible que un gas se convierta en sólido directamente? Sí, esto se llama sublimación inversa y ocurre en ciertos materiales como el hielo seco.
- ¿Por qué el plasma es considerado un estado de la materia? El plasma se considera un estado de la materia porque consiste en partículas cargadas que se comportan de manera diferente a los gases y pueden conducir electricidad.
- ¿Cómo afecta la temperatura a los cambios de estado? La temperatura afecta los cambios de estado al influir en la energía de las partículas; a mayor temperatura, más energía tienen las partículas para moverse y cambiar de estado.